Reacción de oxidación-reducción para ajustar
6. El ![]() en presencia de
en presencia de ![]() transforma el
transforma el ![]() en
en ![]() , formándose también
, formándose también ![]() ,
, ![]() y agua:
y agua:
a) Ajusta la reacción molecular.
b) ¿Cuántos cm3 de disolución de ![]() 0,5 M serán necesarios para reaccionar con 2,40 g de
0,5 M serán necesarios para reaccionar con 2,40 g de ![]() ?
?
a) La reacción que tenemos que ajustar es la siguiente:
![]()
Para ajustarla, calculamos los números de oxidación de cada uno de los elementos:
![]()
La especie que se reduce es el manganeso. La semirreacción de reducción sería:
![]()
Ajustamos los oxígenos con aguas y los hidrógenos con protones. Finalmente, ajustamos la carga con electrones:
![]()
La especie que se oxida es el hierro. La semirreacción de oxidación será:
![]()
En este caso, sólo tenemos que ajustar la carga:
![]()
Multiplicamos la segunda ecuación por cinco para eliminar los electrones y tenemos la reacción iónica global:
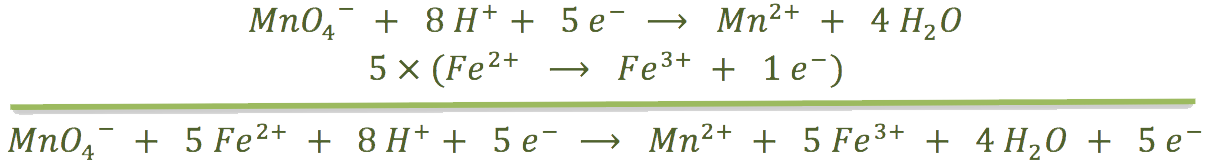
Eliminamos los electrones y ajustamos la ecuación molecular:
![]()
La única sustancia que no aparece en la reacción iónica es el sulfato de potasio, por lo tanto, la tenemos que ajustar al final. Para eso nos fijamos, por ejemplo, en cuantos potasios hay en los reactivos y en los productos. De ahí obtenemos el coeficiente del sulfato de potasio. Si no queremos tener denominadores en el ajuste, podemos multiplicar todos los coeficientes de la reacción por dos:
![]()
b) Nos dan la cantidad que ponemos de un reactivo, el sulfato de hierro, y nos piden el volumen de disolución de permanganato de potasio que se necesita para reaccionar con él:
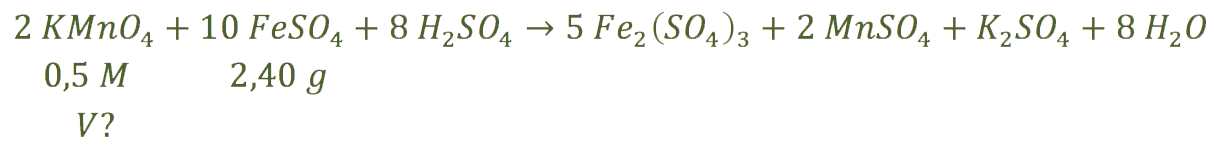
Primero calculamos los moles de sulfato de hierro y a partir de ellos, y con el ajuste de la reacción, los moles que necesitamos de permanganato de potasio:
![]()
![]()
Por último, como sabemos la concentración de la disolución, calculamos el volumen que necesitamos de la misma:
![]()

