Enlaces sigma y enlaces pi
21. Explica razonadamente el tipo de enlace en las siguientes moléculas:
a) Etano.
b) Eteno.
c) Etino.
a) Primero vamos a hacer la estructura de Lewis del etano. Para eso, calculamos los electrones de valencia que tienen entre los 5 átomos:
![]()
El carbono necesita 8 electrones para completar la capa, mientras que el hidrógeno solo 2, así en total se necesitan:
![]()
Si a los electrones que necesitamos le restamos los que tenemos, obtendremos los electrones de enlace:
![]()
Y si a los electrones que tenemos le restamos los electrones de enlace, tendremos los electrones no enlazantes:
![]()
Por lo tanto, la estructura de Lewis será:
.png)
El átomo central, el carbono, tiene la siguiente configuración electrónica:
![]()
Tiene dos electrones desapareados:
![]()
Pero normalmente forma cuatro enlaces y, para poder hacerlo, necesita promocionar un electrón del orbital 2s al 2p para tener otros tantos electrones desapareados. Como son orbitales del mismo nivel, necesita poca energía para poder hacerlo y lo compensa con creces a posteriori cuando forma los cuatro enlaces:
![]()
Los enlaces simples son enlaces ![]() o enlaces frontales donde hay mucho solapamiento de los orbitales que forman parte del enlace, mientras que el enlace doble y el triple son enlaces
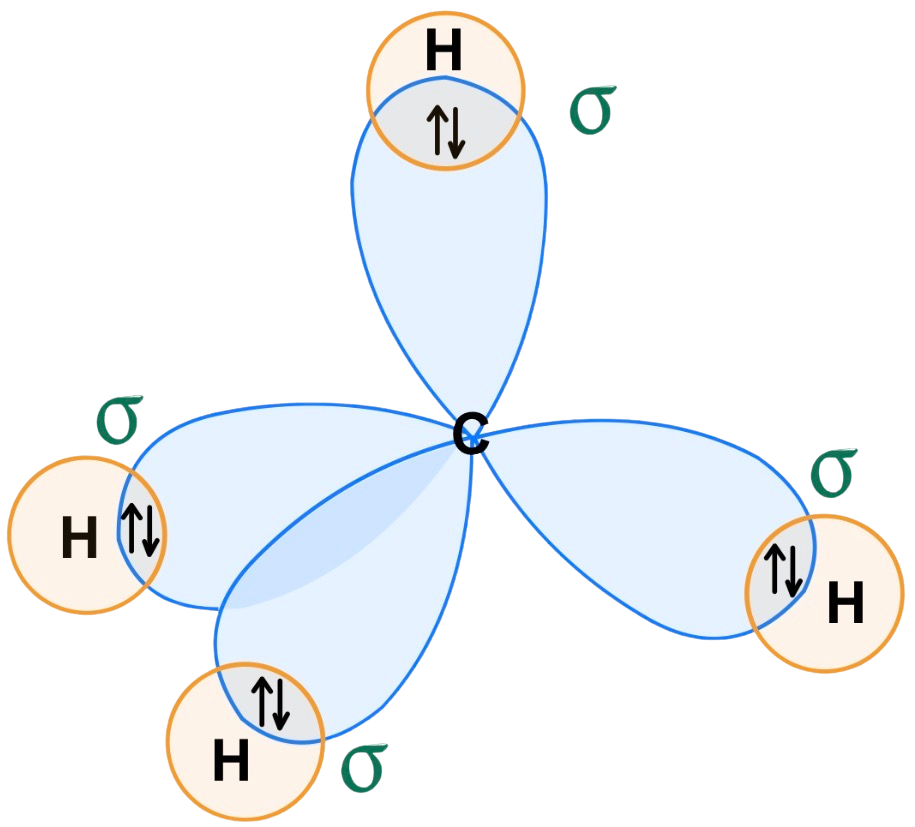
o enlaces frontales donde hay mucho solapamiento de los orbitales que forman parte del enlace, mientras que el enlace doble y el triple son enlaces ![]() o laterales con un solapamiento mucho menor. Estos últimos se forman con orbitales p sin hibridar. En este caso, el carbono no forma ningún enlace doble o triple por lo que no tiene que reservar ningún orbital p. Hibrida todos los orbitales con electrones de valencia, es decir, el 2s y los tres orbitales p. Así la hibridación será sp3. Esos 4 enlaces
o laterales con un solapamiento mucho menor. Estos últimos se forman con orbitales p sin hibridar. En este caso, el carbono no forma ningún enlace doble o triple por lo que no tiene que reservar ningún orbital p. Hibrida todos los orbitales con electrones de valencia, es decir, el 2s y los tres orbitales p. Así la hibridación será sp3. Esos 4 enlaces ![]() se forman entre los 4 orbitales híbridos del carbono y cada uno de los orbitales s del átomo de hidrógeno:
se forman entre los 4 orbitales híbridos del carbono y cada uno de los orbitales s del átomo de hidrógeno:
b) Hacemos la estructura de Lewis del eteno.
![]()
El carbono necesita 8 electrones para completar la capa, mientras que el hidrógeno solo 2, así en total se necesitan:
![]()
Si a los electrones que necesitamos le restamos los que tenemos, obtendremos los electrones de enlace:
![]()
Y si a los electrones que tenemos le restamos los electrones de enlace, tendremos los electrones no enlazantes:
![]()
Por lo tanto, la estructura de Lewis será:
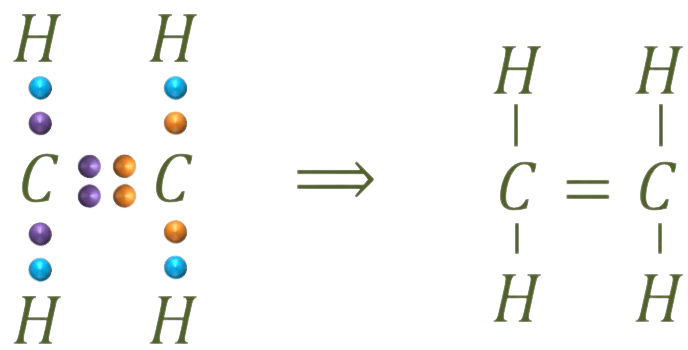
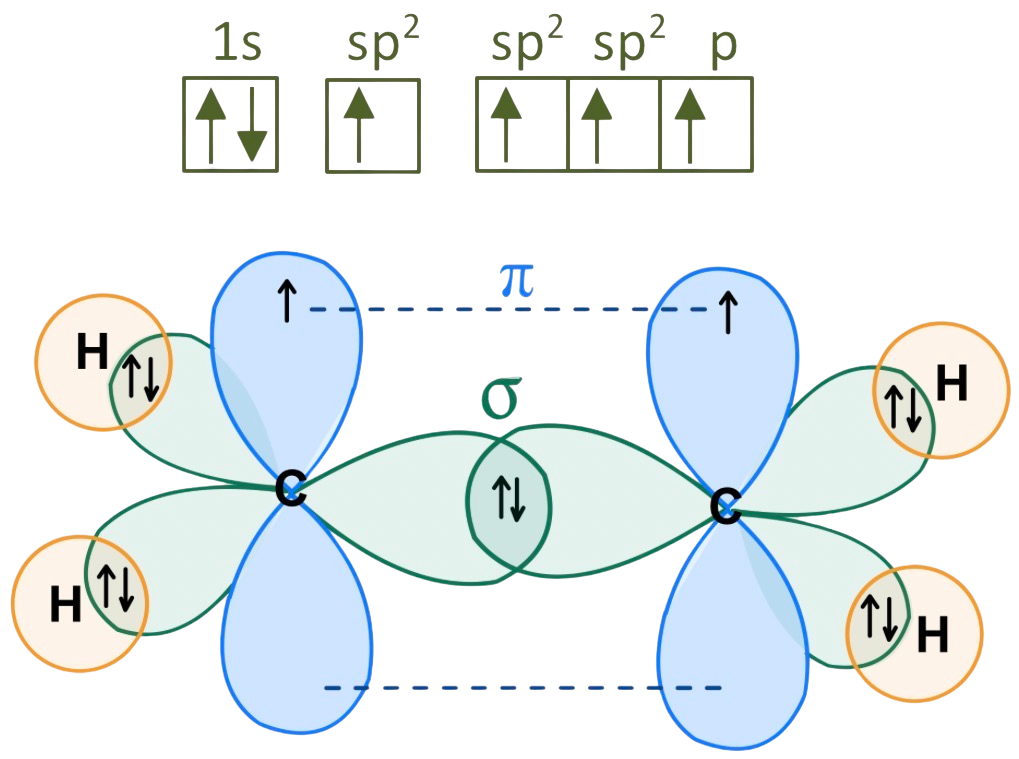
En este caso solo hay que reservar un orbital p para formar el enlace ![]() , el resto de orbitales se hibrida, es decir, un orbital s y dos orbitales p, es decir los carbonos tienen hibridación sp2. Cada carbono forma 3 enlaces
, el resto de orbitales se hibrida, es decir, un orbital s y dos orbitales p, es decir los carbonos tienen hibridación sp2. Cada carbono forma 3 enlaces ![]() (dos con los hidrógenos y uno con el otro carbono) y 1 enlace
(dos con los hidrógenos y uno con el otro carbono) y 1 enlace ![]() (entre los carbonos):
(entre los carbonos):
c) Por último, el etino.
![]()
El carbono necesita 8 electrones para completar la capa, mientras que el hidrógeno solo 2, así en total se necesitan:
![]()
Si a los electrones que necesitamos le restamos los que tenemos, obtendremos los electrones de enlace:
![]()
Y si a los electrones que tenemos le restamos los electrones de enlace, tendremos los electrones no enlazantes:
![]()
Por lo tanto, la estructura de Lewis será:
![]()
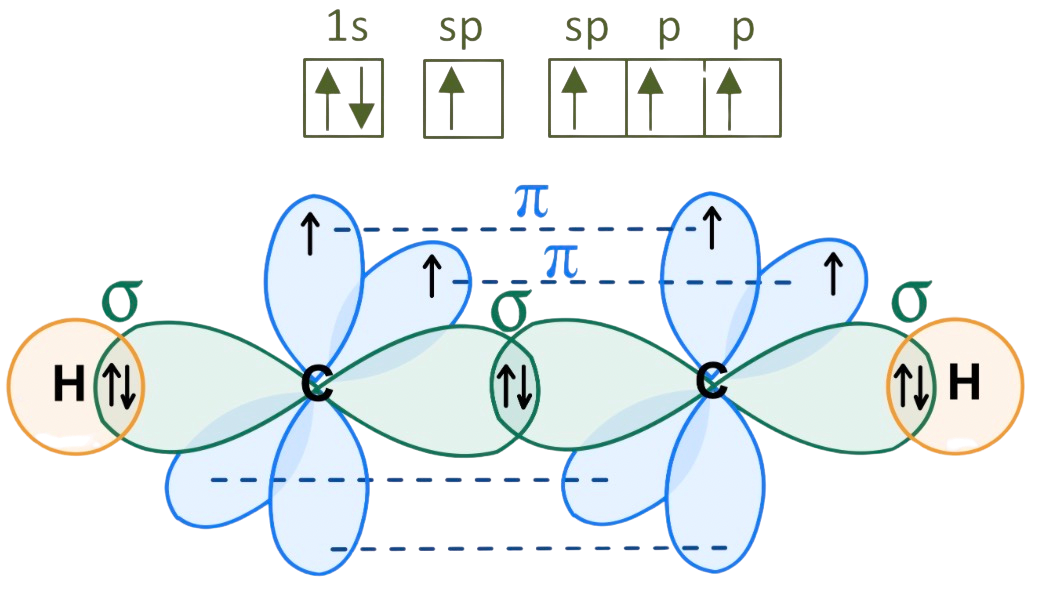
Ahora hay que reservar dos orbitales p para formar los dos enlaces ![]() , el resto de orbitales se hibrida, es decir, un orbital s y un orbitales p, es decir los carbonos tienen hibridación sp. Cada carbono forma 2 enlaces
, el resto de orbitales se hibrida, es decir, un orbital s y un orbitales p, es decir los carbonos tienen hibridación sp. Cada carbono forma 2 enlaces ![]() (uno con el hidrógeno y uno con el otro carbono) y 2 enlace
(uno con el hidrógeno y uno con el otro carbono) y 2 enlace ![]() (entre los carbonos):
(entre los carbonos):