Momento dipolar
14. Dadas las siguientes moléculas: tetracloruro de carbono y tricloruro de boro.
a) Justifica su geometría molecular.
b) Indica qué moléculas presentan momento dipolar.
Razona las respuestas.
a) Primero hacemos la estructura de Lewis de cada una de las moléculas. Comenzamos por el tetracloruro de carbono. Para eso primero calculamos los electrones de valencia que tienen entre los 5 átomos:
![]()
Todos los átomos cumplen la regla del octete, así en total se necesitan:
![]()
Si a los electrones que necesitamos le restamos los que tenemos, obtendremos los electrones de enlace:
![]()
Y si a los electrones que tenemos le restamos los electrones de enlace, tendremos los electrones no enlazantes:
![]()
Por lo tanto, la estructura de Lewis será:
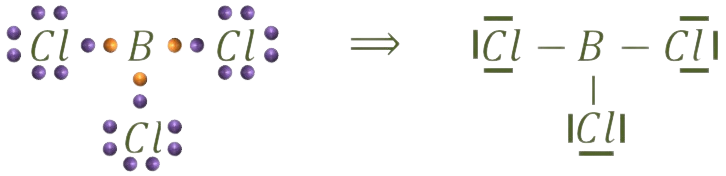
Como vemos, el tetrafluoruro de carbono tiene alrededor del átomo central 4 pares electrónicos enlazantes y ninguno no enlazante y, según la teoría de repulsión de los pares electrónicos de la capa de valencia (TRPECV) esos electrones se colocarían en el espacio lo más separados posible para que las repulsiones sean mínimas. Así tanto la geometría molecular será tetraédrica:
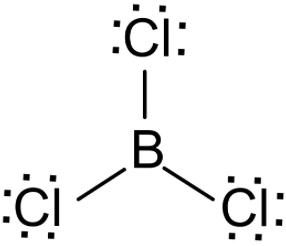
Repetimos el mismo procedimiento para el tricloruro de boro:
![]()
El boro es otro elemento que nunca cumple la regla del octete. Tiene tres electrones de valencia y los comparte, por lo que, al final tiene a su alrededor seis electrones.
![]()
![]()
![]()
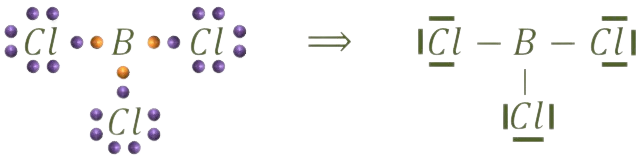
El tricloruro de boro tiene alrededor del átomo central 3 pares electrónicos enlazantes y ninguno no enlazante y, según la teoría de repulsión de los pares electrónicos de la capa de valencia (TRPECV) esos electrones se colocarían en el espacio lo más separados posible para que las repulsiones sean mínimas. Así tanto la geometría molecular será triangular plana:
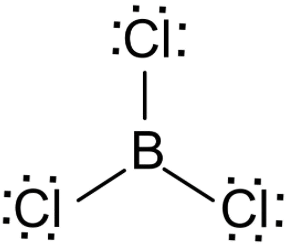
b) Las dos moléculas tienen enlaces polarizados puesto que el cloro es más electronegativo que el carbono y que el boro:
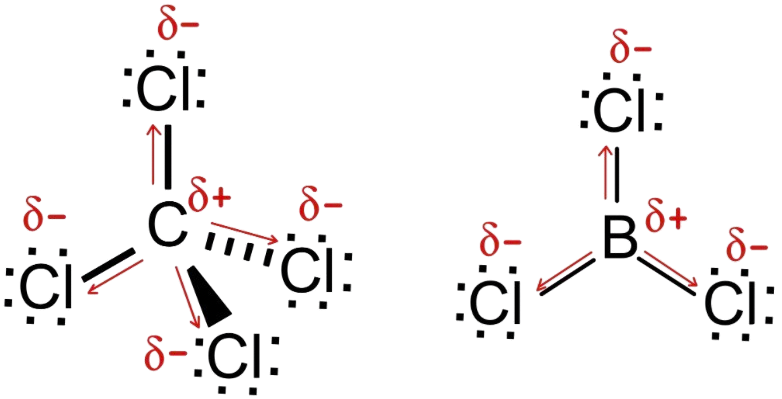
El momento dipolar de cada una de las moléculas es cero (![]() ), puesto que la suma de los vectores de cada una es nula, debido a la geometría. Por lo tanto, tanto el tetracloruro de carbono como el tricloruro de boro son apolares.
), puesto que la suma de los vectores de cada una es nula, debido a la geometría. Por lo tanto, tanto el tetracloruro de carbono como el tricloruro de boro son apolares.

